지난해 하반기 응급 승인 집계…올라파립·리아백스 등 뒤이어
[일요경제 방석현 기자] 지난해 응급 상황에 사용된 의약품들 가운데 사용빈도가 가장 많은 약물로 화이자(Pfizer)의 항암제 로라티닙이 꼽혔다.
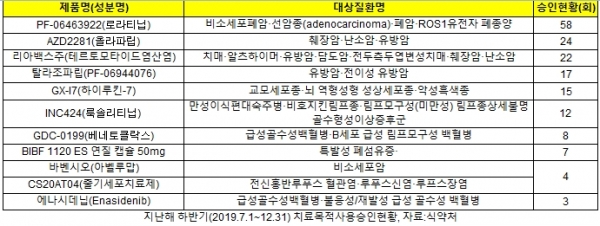
20일 본지가 식품의약품안전처의 지난해 하반기(2019년 7월1일~12월31일) '임상의약품의 치료 목적 사용 승인 현황'분석 결과, 화이자의 3세대 항암제 '로라티닙'이 58건 승인돼 가장 사용빈도가 높은 것으로 나타났다.
이어 아스트라제네카의 항암제 '올라파립'(24건), 삼성제약의 췌장암 신약 '리아백스'(22건), 화이자의 유방암 신약 '탈라조파립'(17건), 제넥신의 항암면역치료제 'GX-I7'(15건), 노바티스의 '룩솔라티닙'(12건) 등이 상위를 차지했다.
임상의약품의 치료 목적 사용 승인은 생명이 위급하거나 다른 치료방법이 없는 환자에게 허가 전 약품을 사용하는 것이다.
로라티닙은 3세대 ALK(역형성 림프종 인산화효소)와 ROS1에 활성을 갖는 약물로 비소세포폐암·선암종(adenocarcinoma)·폐암·ROS1유전자 폐종양 등의 치료에 사용된 것으로 나타났다. 지난해 11월 미국 식품의약국(FDA) 허가를 받았으며, 식약처의 허가도 앞두고 있다.
췌장암·난소암·유방암 치료에 사용된 올라파립은 아스트라제네카의 표적항암제로 지난해 10월 식약처로부터 난소암·유방암에 대한 적응증 추가를 승인 받았다.
지난 2015년 전이성 췌장암 환자의 치료 용도로 조건부 허가를 받은 삼성제약의 항암제 리아백스(테르토모타이드염산염)는 22건 승인됐다. 현재 임상3상 진행 중인 이 약은 췌장암 외에 치매·알츠하이머·유방암·담도암·전두측두엽변성치매·난소암 등에 쓰였다.
탈라조파립은 화이자의 PARP 표적항암제로써 지난해 미국(FDA)과 유럽의약품청(EMA)의 승인을 받았다. 유방암과 전이성 유방암에 특화된 약물이다.
현재 후기 임상1상을 진행중인 제넥신의 GX-I7는 교모세포종·뇌 역형성형 성상세포종·악성흑색종 등의 환자 처방에 사용됐다. 지난해 미국 면역항암제 학회(SITC 2019)에서 말기 고형암 환자들 대상의 유의미한 개선 결과가 발표되기도 했다.
노바티스의 신약후보약물인 INC424(룩솔리티닙)의 경우, 만성이식편대숙주병·비호지킨림프종·림프모구성(미만성)·림프종상세불명 골수형성이상증후군 등에 쓰여 활용범위가 가장 넓었다.
이밖에 베네토클락스(애브비, 8건), 오페브(베링거인겔하임, 7건), 아벨루맙·CS20AT04(4건), 에나시데닙(셀진, 3건) 등도 응급환자에게 처방된 것으로 나타나 빠른 허가가 기대되는 약물로 꼽혔다.
업계 관계자는 "임상 중인 의약품들 치료법이 없는 일부 환자들에게 유용하게 처방되고 있는 만큼 해당 약품의 빠른 허가로 환자들의 시름을 덜어주길 기대한다"고 말했다.

